在非人灵长类研究中,一个常被忽视却极具转化意义的事实是:猴子的基础血尿酸水平远低于人类。研究显示,恒河猴的血尿酸基线水平约为人类的十分之一。这一差异并非实验条件造成,而是源于灵长类进化过程中一次关键的遗传分化。
在药物研发实践中,研究人员常发现:某些在猴子模型中表现出良好降尿酸效果的化合物,在进入人体临床后却疗效有限甚至失败。其根本原因,正是人类与猴子在尿酸代谢通路上的本质差异。
进化分水岭:尿酸酶的失活
绝大多数哺乳动物(包括非人灵长类)体内仍保留功能性尿酸酶(uricase),可将尿酸进一步氧化为高度水溶性的尿囊素,从而维持较低的血尿酸水平。
分子系统发育研究表明,在约 2000–3000 万年前,人类与类人猿共同祖先的尿酸酶基因发生关键突变,导致其催化活性逐步下降并最终完全失活。自此,尿酸成为人类嘌呤代谢的终产物,并在体内更易积累。
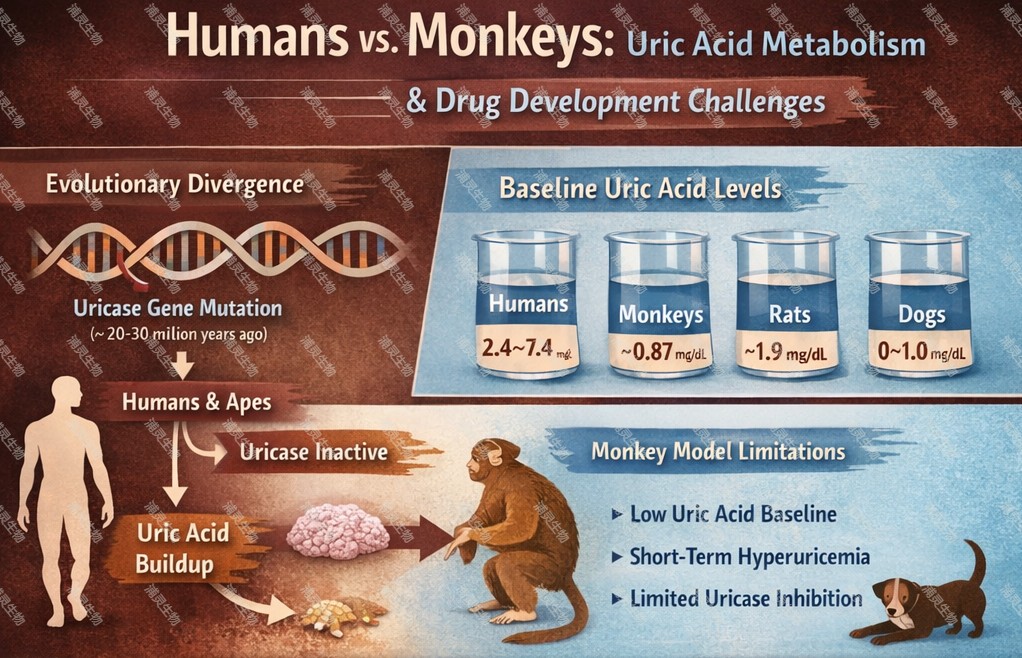
不同物种的尿酸水平对比
典型血清尿酸水平显示出显著的物种差异:
人类:约 2.4–7.4 mg/dL
恒河猴:约 0.87 mg/dL
大鼠:约 2.0 mg/dL
犬:0–1.0 mg/dL
这种差异不仅是数值层面的,更反映了代谢终点的不同。人类更容易出现长期高尿酸状态,而猴子则天然维持在低尿酸水平。
痛风阈值与模型局限
在人类中,当血尿酸持续高于约 6.8 mg/dL(37°C) 时,尿酸钠可能在关节液中结晶,引发痛风。然而,猴子由于具备功能性尿酸酶,即使在外源性诱导条件下,也很难达到这一阈值。
研究表明,即便给予恒河猴高剂量肌苷,其血尿酸峰值仍明显低于人类痛风相关水平。这意味着,常规猴模型难以模拟人类慢性高尿酸血症及痛风的病理过程。
对药物研发的启示
这一代谢差异对降尿酸药物和相关代谢药物的研发具有重要影响。多数实验动物(包括非人灵长类)并不天然处于高尿酸状态,使得动物实验结果在向人体外推时存在明显不确定性。
通过尿酸酶抑制剂或嘌呤前体物质,可在猴子中建立急性高尿酸模型,用于药效初筛和机制验证,但此类模型通常为短期、可逆状态,难以反映人类长期代谢异常。
食蟹猴在代谢研究中的真实价值
尽管在尿酸代谢方面存在差异,食蟹猴在整体代谢和药物转化研究中仍具有不可替代的价值。
在浦灵生物的代谢类疾病研究平台中,食蟹猴广泛应用于肥胖、胰岛素抵抗、脂代谢异常及脂肪性肝病等模型。这些模型在以下方面与人类高度相关:
药物代谢与药代动力学(PK)特征
肾脏与全身代谢生理结构
系统性代谢调控及安全性评估
对于间接影响尿酸水平的代谢通路(如果糖代谢、脂质代谢或肾脏转运机制),食蟹猴模型仍可提供重要的机制性与转化性信息。

肾脏处理机制的差异
除尿酸酶外,人类与猴子在肾脏尿酸处理方面亦存在差异。人类肾脏中约 90% 的滤过尿酸会被重新吸收,这种“保留机制”进一步放大了高尿酸风险;而猴子由于总体尿酸负荷较低,其肾脏转运特征与人类并不完全一致。
因此,靶向肾脏尿酸转运蛋白的药物,在猴子与人体中的药效表现和 PK 特征可能存在显著差异。
结语
尿酸代谢的物种差异,是进化留给现代药物研发的重要提醒。亲缘关系接近,并不等同于代谢路径一致。
在临床前研究中,关键并非“是否使用动物模型”,而是是否理解模型所代表的生物学边界。当一种药物在动物实验中表现优异时,或许更值得追问的是:
使用的是哪一种动物?它的代谢终点是否真正接近人类?
这一答案,往往决定了药物能否真正走向临床成功。

Get in Touch
*We respect your confidentiality and all information are protected.
